2021年CDE受理1439個藥品申報,中藥創(chuàng)新高、生物制品勢頭強勁
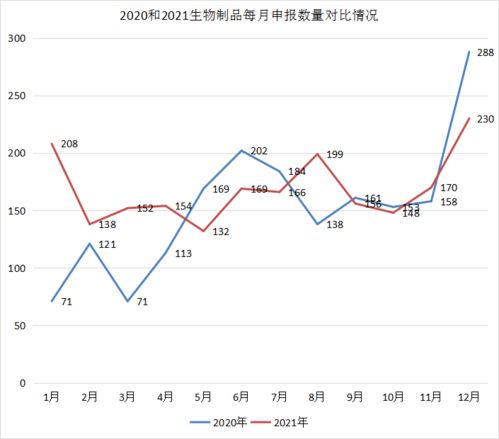
2021年,國家藥品監(jiān)督管理局藥品審評中心(CDE)共受理藥品注冊申請1439個,這一數(shù)據(jù)反映了我國醫(yī)藥行業(yè)的創(chuàng)新活力與政策引導(dǎo)成效。其中,中藥申報數(shù)量創(chuàng)下歷史新高,生物制品領(lǐng)域亦展現(xiàn)出強勁的發(fā)展勢頭,共同構(gòu)成了年度藥品審評的亮點。
一、總體受理情況:創(chuàng)新藥占比提升,審評效率持續(xù)優(yōu)化
2021年CDE受理的1439個藥品注冊申請中,創(chuàng)新藥和改良型新藥占比顯著提高,體現(xiàn)了我國從“仿制為主”向“創(chuàng)新驅(qū)動”的戰(zhàn)略轉(zhuǎn)型。CDE通過優(yōu)先審評、突破性治療藥物程序等機制,加速了臨床急需和具有明顯臨床價值的藥品上市。同時,審評流程的數(shù)字化、標準化建設(shè)進一步提升了效率,為企業(yè)和研發(fā)機構(gòu)提供了更加明確和可預(yù)期的審評環(huán)境。
二、中藥申報數(shù)量創(chuàng)新高:政策紅利釋放,研發(fā)熱情高漲
2021年,中藥注冊申報數(shù)量達到近年峰值,這主要得益于多項支持中醫(yī)藥發(fā)展的政策落地。例如,《中藥注冊分類及申報資料要求》的實施,明確了中藥創(chuàng)新藥、改良型新藥、經(jīng)典名方等分類,簡化了申報流程,激發(fā)了企業(yè)的研發(fā)積極性。新冠疫情中中醫(yī)藥的廣泛應(yīng)用,也提升了市場對中藥價值的認可,促使更多企業(yè)投入中藥新藥研發(fā)。經(jīng)典名方制劑、中藥復(fù)方制劑以及源于古代經(jīng)典名方的中藥新藥成為申報熱點,展現(xiàn)了中藥現(xiàn)代化與標準化進程的加速。
三、生物制品領(lǐng)域:創(chuàng)新突破頻現(xiàn),研發(fā)管線豐富
生物制品作為醫(yī)藥創(chuàng)新的前沿領(lǐng)域,在2021年表現(xiàn)尤為突出。CDE受理的生物制品申請覆蓋了單克隆抗體、細胞治療、基因治療、疫苗等多個細分領(lǐng)域。其中,腫瘤免疫治療藥物(如PD-1/PD-L1抑制劑)持續(xù)領(lǐng)跑,CAR-T細胞治療等前沿技術(shù)亦有多項申請進入審評階段。新冠疫情推動疫苗研發(fā)加速,多款mRNA疫苗、重組蛋白疫苗等新型疫苗申報,彰顯了我國生物制藥技術(shù)的快速進步。生物類似藥的申報數(shù)量穩(wěn)步增長,顯示出國內(nèi)企業(yè)在生物藥研發(fā)與產(chǎn)業(yè)化方面的成熟度提升。
四、趨勢展望:中藥與生物制品或成未來增長雙引擎
綜合2021年數(shù)據(jù),中藥與生物制品已成為我國藥品研發(fā)的兩大增長點。中藥在政策扶持與市場需求雙重驅(qū)動下,有望在慢性病管理、抗病毒等領(lǐng)域?qū)崿F(xiàn)更大突破;生物制品則憑借技術(shù)迭代與臨床優(yōu)勢,將持續(xù)引領(lǐng)創(chuàng)新藥發(fā)展。未來,CDE或進一步優(yōu)化審評策略,鼓勵中西醫(yī)結(jié)合、生物技術(shù)與傳統(tǒng)醫(yī)藥融合的創(chuàng)新路徑,為全球醫(yī)藥貢獻更多“中國方案”。
2021年CDE受理數(shù)據(jù)的亮眼表現(xiàn),不僅是我國醫(yī)藥創(chuàng)新能力的體現(xiàn),更是政策環(huán)境、市場需求與技術(shù)積累共同作用的結(jié)果。中藥申報創(chuàng)新高與生物制品的蓬勃發(fā)展,預(yù)示著我國醫(yī)藥產(chǎn)業(yè)正邁向更加多元化、高質(zhì)量的創(chuàng)新階段。
如若轉(zhuǎn)載,請注明出處:http://www.miyuys.cn/product/10.html
更新時間:2026-04-18 16:22:21